Proteomics - Mir Biotech
Използвахме нов подход за идентифициране на функционално важни микроРНК (miRNA) -целеви взаимодействия, интегриращи miRNA, транскриптомни и протеомни профили и усъвършенствани in silico анализ, използвайки алгоритъма FAME. Тъй като miRNAs играят решаваща роля във вътрешното ухо, демонстрирано от откриването на мутации в miRNA, водещи до глухота при хора и мишки, ние приложихме този подход към микродисектиран слухов и вестибуларен сензорен епител. Открихме експресията на 157 miRNAs в сензорния епител на вътрешното ухо, с 53 miRNAs, различно експресирани между кохлеята и вестибула.
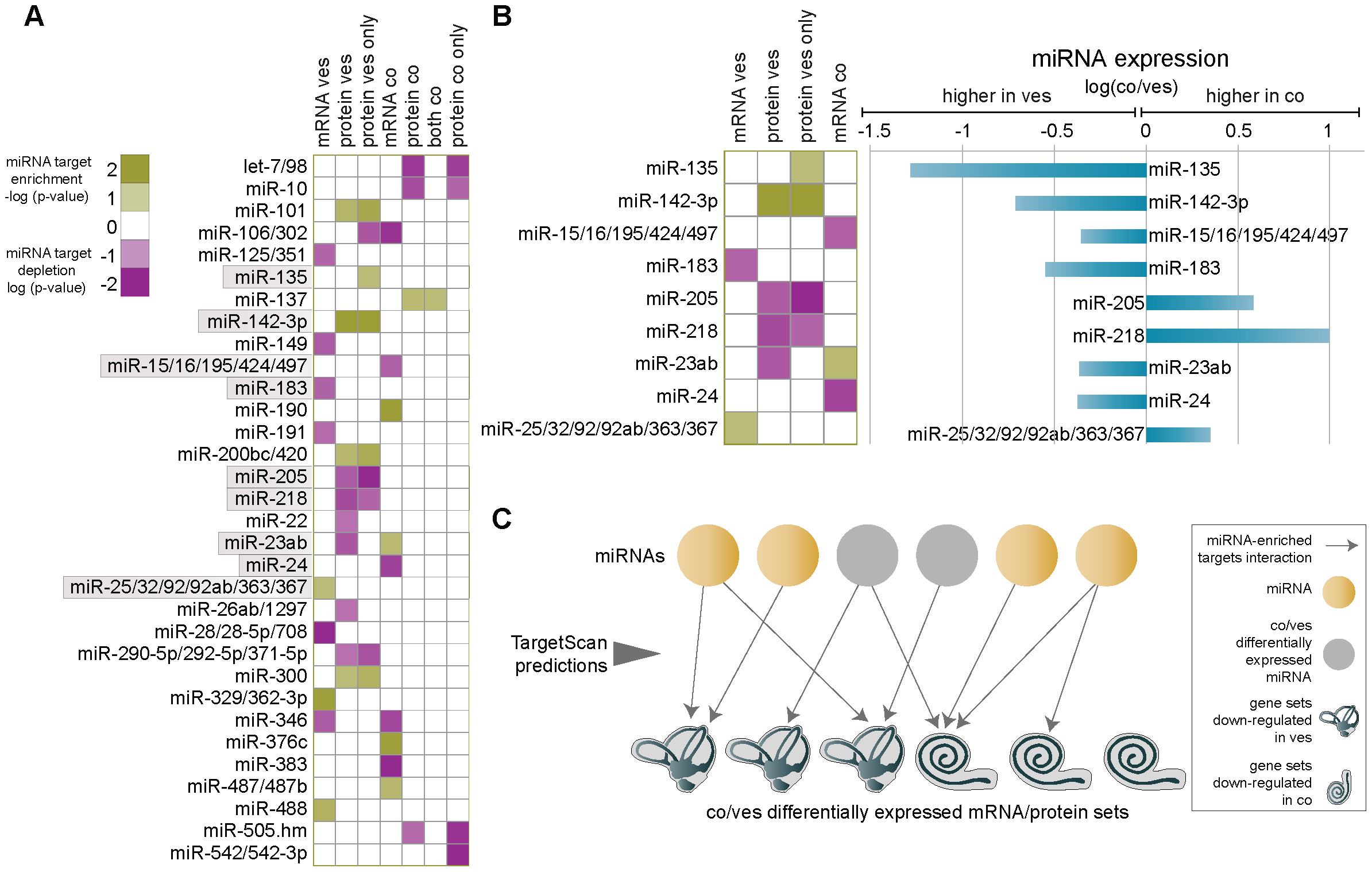
Функционално важните miRNAs бяха определени чрез търсене на обогатени или изчерпани мишени в наборите от данни за транскрипт и протеини с експресия, съответстваща на догмата за регулацията на miRNA. Важно е, че доста от мишените бяха открити само в наборите от данни за протеини, дължащи се на регулация чрез потискане на транслацията. Ние идентифицирахме и експериментално потвърдихме регулацията на PSIP1-P75, транскрипционен коактиватор, неизвестен преди това във вътрешното ухо, чрез miR-135b, във вестибуларни космени клетки. Нашите открития показват, че miR-135b служи като клетъчен ефектор, участващ в регулирането на някои от разликите между кохлеарните и вестибуларните космени клетки.
МикроРНК (miRNAs) са малки (17-24 нуклеотидни дълги) некодиращи РНК, обработени от транскриптите на ендогенни гени, които функционират по пътя на интерференцията на РНК (RNAi) [1]. По -специално, чрез свързване към последователности в 3 'нетранслираната област (UTR) на гени, miRNA може да инхибира целевите иРНК. Инхибирането се осъществява или чрез транслационно потискане и дестабилизиране на тРНК на иРНК с несъвършени комплементарни последователности, често срещани при бозайници, или чрез разцепване на иРНК с перфектно съвпадение с тяхната последователност, често срещана при растенията [2], [3]. В първия се смята, че запазеното сдвояване към 5 ′ областта на miRNA центровете върху нуклеотиди 2–7, наречени „семена“, е важно за разпознаването на миРНК мишена [2]. Към днешна дата приблизително 200 широки еволюционно консервирани семейства miRNA и стотици допълнителни слабо консервирани miRNAs са идентифицирани при бозайници [4]. Изчислено е, че приблизително две трети от всички гени, кодиращи човешки протеин, са консервативни мишени на miRNAs [5]; следователно miRNA осигуряват широко разпространен механизъм за посттранскрипционен контрол на генната експресия. miRNAs са замесени в множество биологични процеси, включително развитие и диференциация, пролиферация, онкогенеза, възпаление, хематопоеза и ангиогенеза [6] - [10]. Наскоро беше установено, че мутация в miR-96 е в основата на наследствена загуба на слуха при хора [11] и мишки [12]. Към днешна дата това е единственият докладван пример за muRNA мутация, причиняваща Менделска болест.
Класическият подход към разбирането на биологичните роли на miPHK е да се идентифицират техните цели и да се проучи тяхната функция в съответната система. Въпреки това, методите за предсказване на миРНК мишени се оказаха основна бариера в областта, главно поради непълно разбиране на взаимодействието на прицелен ген, свързващ миРНК. Докато изчислителните алгоритми за прогнозиране на мишени предоставят големи списъци с предложени миРНК цели, сравнително ограничен брой е валидиран.
За да се подобри вероятността за идентифициране на биологично значими мишени, проучванията често използват анализ на микрочипове, за да определят профилите на експресия на miRNAs и техните прогнозирани целеви иРНК (напр. [8], [13], [14]). Въпреки че последните проучвания показват, че репресията на протеините често се отразява от намалените нива на транскрипция на миРНК мишени [15] - [17], са идентифицирани и примери, при които транслационната репресия е основният компонент на заглушаването [17] - [19]. Следователно, изучаването както на нивата на тРНК, така и на протеина дава най -информативна представа за регулацията на miRNA и техните функционални роли в определени тъкани или органи.